Quy trình nuôi cấy tế bào gốc trung mô trong phòng thí nghiệm
Tế bào gốc trung mô (MSC) là những tế bào đa năng có khả năng sinh sôi và thay thế các tế bào chết trong cơ thể. MSC có thể dễ dàng được phân lập và nuôi cấy trong phòng thí nghiệm cho nhiều ứng dụng khác nhau. Ở bài viết này, Mescells sẽ cung cấp các thông tin về quy trình nuôi cấy tế bào gốc trung mô, vai trò, điều kiện cần thiết và thách thức trong quá trình nuôi cấy loại tế bào này.
1. Vai trò của nuôi cấy tế bào gốc trung mô
Nuôi cấy tế bào gốc trung mô (MSC) đóng vai trò cốt lõi trong y học tái tạo, giúp tăng sinh số lượng lớn từ nhiều nguồn như mô mỡ, dây rốn… để điều trị hơn 100 loại bệnh, bao gồm thoái hóa khớp, bệnh tự miễn, đái tháo đường và tổn thương mô.

Mục tiêu chính của việc nuôi cấy tế bào gốc trung mô (MSC):
Tăng sinh và sản xuất quy mô lớn: Nuôi cấy giúp biến một lượng nhỏ tế bào gốc ban đầu thành số lượng lớn (hàng trăm triệu đến hàng tỷ tế bào), đủ để đáp ứng cho các liệu pháp điều trị đa liều hoặc nhiều lần.
Biệt hóa thành các loại tế bào chuyên biệt: Trong môi trường nuôi cấy phù hợp, MSC được biệt hóa thành tế bào xương, sụn, mỡ, cơ hoặc tế bào thần kinh, ứng dụng trong tái tạo mô bị tổn thương.
Điều hòa miễn dịch và chống viêm: MSC nuôi cấy có khả năng giảm viêm, điều hòa hệ miễn dịch, làm giảm nguy cơ thải ghép trong các ca ghép đồng loài và điều trị bệnh tự miễn.
Sửa chữa và tái tạo mô: Tế bào gốc được nuôi cấy tiết ra các yếu tố tăng trưởng, thúc đẩy quá trình chữa lành các mô bị hỏng (trong các trường hợp xơ gan, phổi tắc nghẽn, suy tim…).
Chống lão hóa và thẩm mỹ: MSC có khả năng kích thích sản sinh collagen và elastin, giúp làm chậm quá trình lão hóa và phục hồi chức năng cơ thể
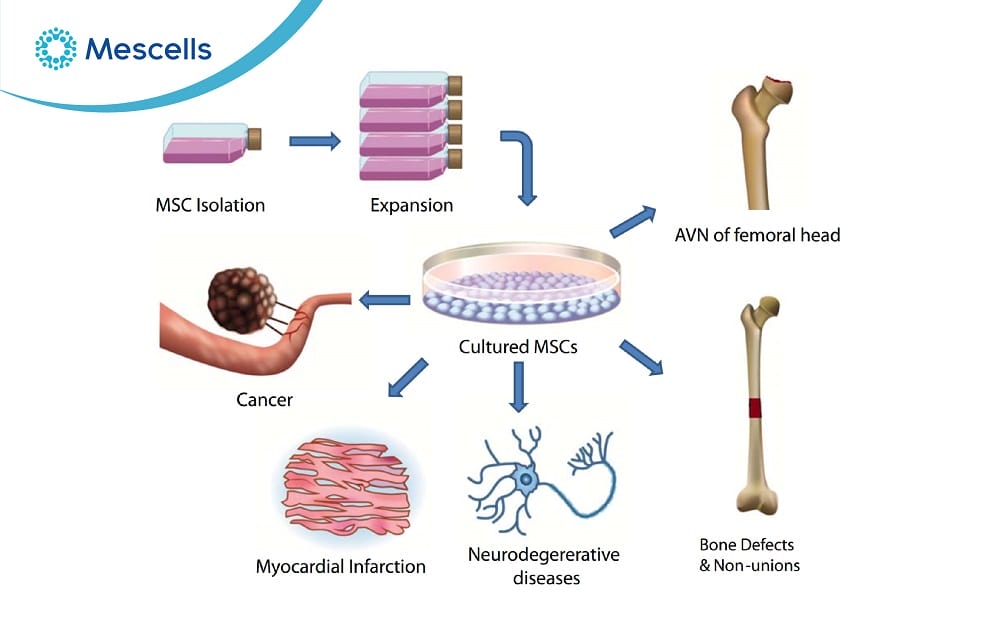
Nuôi cấy tế bào gốc trung mô nhằm mở rộng và tăng sinh số lượng lớn tế bào phục vụ điều trị bệnh lý
2. Điều kiện cần thiết để nuôi cấy tế bào gốc trong phòng thí nghiệm
Nuôi cấy tế bào là kỹ thuật được sử dụng để duy trì và tăng sinh tế bào trong điều kiện phòng thí nghiệm có kiểm soát. Để đạt được kết quả tốt, quá trình này đòi hỏi phải đáp ứng một số điều kiện và kỹ thuật nhất định nhằm đảm bảo khả năng sống sót và phát triển của tế bào.
2.1. Môi trường nuôi cấy
Tế bào cần được cung cấp các chất dinh dưỡng và yếu tố tăng trưởng thích hợp để tồn tại và tăng sinh. Môi trường nuôi cấy là hỗn hợp gồm các muối, axit amin, vitamin, huyết thanh hoặc chất thay thế huyết thanh và các phụ gia khác.
Tùy từng loại tế bào gốc, môi trường nuôi cấy sẽ khác nhau. Ví dụ, tế bào gốc phôi người và tế bào gốc đa năng cảm ứng (iPSC) thường được nuôi trong môi trường nền như DMEM/F12 và cần bổ sung các yếu tố tăng trưởng như yếu tố tăng trưởng nguyên bào sợi cơ bản (bFGF/FGF2) để duy trì trạng thái chưa biệt hóa. Trong khi đó, tế bào gốc phôi chuột thường cần bổ sung yếu tố ức chế bệnh bạch cầu (LIF).
2.2. Điều kiện nuôi cấy
Để nuôi cấy tế bào gốc thành công, cần tạo ra môi trường nuôi cấy phù hợp và duy trì các điều kiện vật lý ổn định. Điều này bao gồm kiểm soát vô trùng, nhiệt độ, độ ẩm, độ pH, nồng độ oxy và carbon dioxide.
Môi trường vô trùng là yêu cầu bắt buộc nhằm ngăn ngừa vi khuẩn, nấm hoặc các vi sinh vật khác phát triển và cạnh tranh với tế bào về chất dinh dưỡng và không gian. Vì vậy, toàn bộ dụng cụ, bề mặt làm việc và môi trường nuôi cấy phải được làm sạch, khử trùng, đồng thời các thao tác phải thực hiện trong điều kiện vô trùng nghiêm ngặt.
Nhiệt độ tối ưu cho phần lớn tế bào động vật có vú, bao gồm nhiều loại tế bào gốc, là 37°C. Độ ẩm trong tủ nuôi cấy thường được duy trì ở khoảng 95% để hạn chế bay hơi môi trường. Độ pH của môi trường cũng cần được giữ ổn định, thường trong khoảng 7,2-7,4, nhằm đảm bảo hoạt động trao đổi chất và sự phát triển bình thường của tế bào.

Quy trình nuôi cấy tế bào gốc trong phòng thí nghiệm đòi hỏi các điều kiện nghiêm ngặt
Ngoài ra, nồng độ oxy có ảnh hưởng quan trọng đến khả năng tăng sinh và duy trì trạng thái chưa biệt hóa của tế bào gốc. Một số loại tế bào gốc, đặc biệt là tế bào gốc phôi, tế bào gốc đa năng cảm ứng và tế bào gốc trung mô, thường phát triển tốt hơn trong điều kiện oxy thấp hơn so với không khí thông thường, thường khoảng 1-5% O2. Điều kiện này giúp duy trì tính đa tiềm năng và hạn chế biệt hóa sớm.
Nồng độ CO2 phải cân bằng với nồng độ natri bicarbonat cao trong môi trường nuôi cấy thông thường để tạo thành hệ đệm và cân bằng độ pH của môi trường. Nếu không có CO2 trong hệ thống nuôi cấy, natri bicarbonat trong môi trường nuôi cấy thông thường có thể bị phân hủy thành natri cacbonat, dẫn đến tăng độ pH trong môi trường và gây chết tế bào (1).
2.3. Giá thể nuôi cấy
Một trong những yêu cầu thiết yếu đối với nuôi cấy tế bào gốc là chất nền tăng trưởng phù hợp, cung cấp bề mặt cho tế bào bám dính và phát triển. Việc lựa chọn chất nền phụ thuộc vào loại tế bào được nuôi cấy và ứng dụng dự định. Có nhiều loại chất nền tăng trưởng khác nhau, bao gồm nhựa, thủy tinh và các lớp phủ chuyên dụng như collagen hoặc fibronectin.
3. Quy trình nuôi cấy tế bào gốc trung mô trong phòng thí nghiệm
Các bước chi tiết trong quy trình nuôi cấy tế bào gốc trung mô (2):
3.1. Thu thập và vận chuyển mẫu
Mẫu mô (như mô mỡ, mô dây rốn, hoặc tủy xương) được thu thập trong điều kiện vô trùng và vận chuyển nhanh chóng đến phòng thí nghiệm trong môi trường bảo quản chuyên dụng.
3.2. Phân lập tế bào gốc (MSC)
- Phương pháp Enzyme: Sử dụng các loại enzyme như Collagenase để phân hủy mô, giải phóng tế bào.
- Phương pháp mảnh mô (Explant): Mảnh mô được đặt trực tiếp vào chai nuôi cấy, tế bào gốc sẽ tự di cư ra ngoài.
- Loại bỏ hồng cầu: Sử dụng dung dịch ly giải hồng cầu để làm sạch mẫu.
3.3. Nuôi cấy sơ cấp (Primary Culture)
- Tế bào sau khi phân lập được gieo vào các chai nuôi cấy (ví dụ T-25, T-75) cùng môi trường tăng sinh chuyên dụng (thường chứa DMEM/F12, huyết thanh bò thai FBS).
- Ủ tế bào ở 37 độ C và 5% CO2.
- Thay môi trường lần đầu sau 24-48 giờ để loại bỏ tế bào không bám dính.
3.4. Tăng sinh và cấy chuyển (Passage)
- Thay môi trường định kỳ (2-3 ngày/lần) cho đến khi tế bào bám dính và đạt độ bao phủ khoảng 80-90%.
- Sử dụng Trypsin-EDTA để tách tế bào khỏi bề mặt nuôi cấy, sau đó cấy chuyển sang chai lớn hơn (nhân giống) hoặc thu hoạch.
3.5. Kiểm tra chất lượng và lưu trữ
Kiểm tra chất lượng
– Xác định số lượng tế bào sống: Sử dụng thuốc nhuộm đặc biệt để kiểm tra, nếu đạt mật độ ≥90% tế bào còn sống sẽ đủ dùng cho điều trị.
– Định danh tế bào gốc trung mô (MSC) theo tiêu chuẩn của hiệp hội Quốc tế về Liệu pháp Tế bào và Gen (ISCT) dựa trên ba tiêu chí tối thiểu:
- Khả năng bám dính tốt vào bề mặt nhựa trong chai nuôi cấy.
- Biểu hiện kháng nguyên bề mặt đặc hiệu. Có thể sử dụng kỹ thuật Flow Cytometry để kiểm tra các dấu ấn bề mặt đặc trưng (CD73+, CD90+, CD105+, CD34-, CD45-, HLA-DR).
- Biệt hóa thành ba dòng tế bào trong ống nghiệm (tế bào tạo xương, tế bào mỡ, tế bào tạo sụn).
– Kiểm tra độ vô khuẩn (nuôi cấy 14 ngày không vi khuẩn/nấm), nội độc tố (≤5 EU/mL – không gây sốt), mycoplasma (không phát hiện) và bộ gene bình thường (không đột biến).
Lưu trữ
Tế bào được trộn với dung dịch bảo quản (CryoStore) và hạ nhiệt độ từ từ để thực hiện quy trình bảo quản lạnh lâu dài. Quá trình này có thể bảo quản tế bào gốc từ vài tháng đến vài chục năm, tùy theo nhu cầu của mục đích nuôi cấy
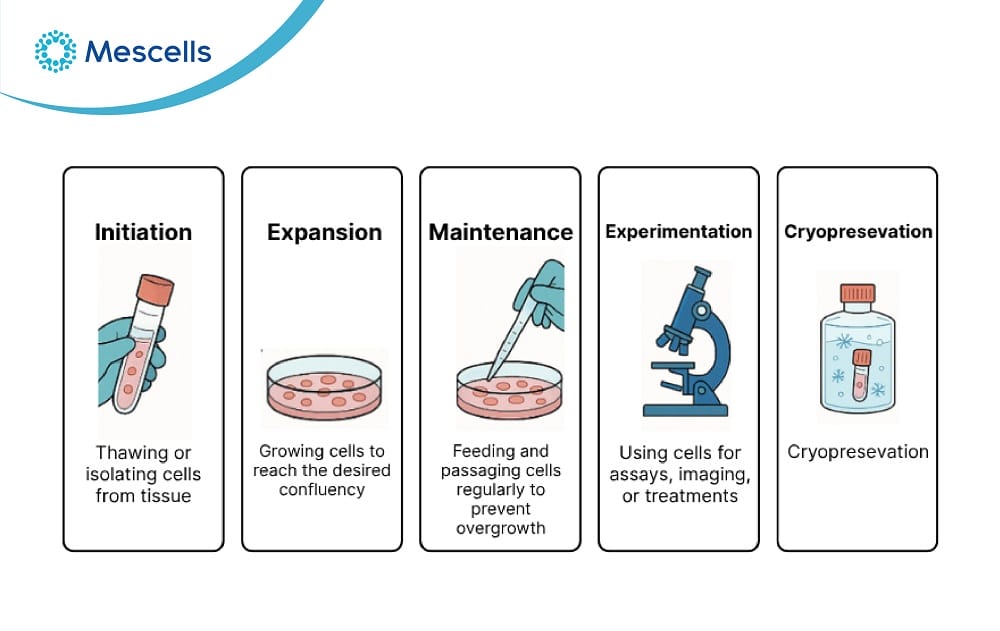
Các bước cơ bản của quy trình nuôi cấy tế bào gốc trong phòng thí nghiệm
4. Thách thức trong nuôi cấy tế bào gốc trung mô
Nuôi cấy tế bào gốc trung mô phải đối mặt với những thách thức đáng kể liên quan đến việc duy trì các đặc tính vốn có của chúng như khả năng tự làm mới, tính đa tiềm năng, đảm bảo tính ổn định di truyền và đạt được sự biệt hóa nhất quán trên quy mô lớn. Cụ thể như sau:
Duy trì các đặc tính của tế bào gốc
Việc đảm bảo tế bào gốc duy trì khả năng tự tái tạo và tiềm năng (đa năng) trong quá trình nuôi cấy dài hạn mà không bị biệt hóa sớm là điều khó khăn. Một trong những yếu tố quan trọng của bất kỳ phương pháp nuôi cấy nào là các tế bào được nuôi cấy phải có khả năng sống tối ưu và thể hiện hoạt động chức năng tương đương với các tế bào được tìm thấy trong cơ thể sống. Những tế bào này cũng phải có khả năng tồn tại và tích hợp vào mô trong cơ thể sống (3).
Tính ổn định di truyền và kiểm soát chất lượng
Tế bào gốc có thể tích lũy các bất thường và đột biến di truyền trong quá trình tăng sinh mạnh mẽ trong ống nghiệm. Việc xác định những thay đổi này đòi hỏi các phương pháp phân tích nghiêm ngặt.
Nguy cơ nhiễm khuẩn
Các mẫu nuôi cấy dễ bị nhiễm khuẩn bởi vi khuẩn, nấm, mycoplasma, virus và có thể ảnh hưởng đến toàn bộ dòng tế bào. Trong nuôi cấy tế bào, sự nhiễm bẩn có thể đến từ các nguồn hóa học và sinh học. Các dấu hiệu của sự nhiễm bẩn này thường bao gồm tăng trưởng tế bào chậm, bất thường về hình thái, thay đổi pH đột ngột trong môi trường nuôi cấy và nồng độ tế bào chết hoặc tế bào trôi nổi cao hơn trong môi trường nuôi cấy. Việc sàng lọc thường xuyên các chất ô nhiễm này trong nuôi cấy tế bào là rất quan trọng để đảm bảo tính nhất quán của kết quả và ngăn ngừa những hậu quả có thể gây hại (4).

Tối ưu quy trình bảo quản lạnh một cách hiệu quả là thách thức trong nuôi cấy tế bào gốc trung mô
Mở rộng quy mô sản xuất
Việc chuyển từ nuôi cấy đơn lớp 2D sang môi trường lò phản ứng sinh học 3D là cần thiết để sản xuất dược phẩm quy mô lớn, tiết kiệm chi phí, nhưng điều này lại gặp nhiều thách thức về mặt kỹ thuật.
Tính không đồng nhất và hiệu quả biệt hóa
Quần thể tế bào gốc thường không đồng nhất, dẫn đến sự biệt hóa không nhất quán thành các loại tế bào mong muốn.
Sử dụng nguyên liệu có nguồn gốc từ động vật
Nhiều quy trình truyền thống dựa vào tế bào nuôi cấy hoặc huyết thanh có nguồn gốc từ động vật, điều này gây ra sự biến đổi và nguy cơ lây truyền mầm bệnh, khiến việc xin phê duyệt theo quy định trở nên khó khăn hơn.
Hạn chế của phương pháp bảo quản lạnh
Việc đông lạnh và rã đông một lượng lớn tế bào gốc biệt hóa chuyên biệt trong khi vẫn duy trì khả năng sống của chúng khó khăn hơn so với các dòng tế bào thông thường.
Vấn đề an toàn (Khả năng gây ung thư)
Tế bào gốc vạn năng có nguy cơ hình thành u quái (khối u) nếu các tế bào chưa biệt hóa vẫn còn tồn tại trong quần thể tế bào dự định cấy ghép.
Tế bào gốc là công cụ hữu hiệu để phát triển liệu pháp tế bào và y học tái tạo, đem lại cơ hội điều trị nhiều bệnh lý, đặc biệt là các bệnh hiểm nghèo. Trong tương lai, việc tối ưu quy trình nuôi cấy tế bào gốc trung mô kết hợp với kiểm soát chặt chẽ chất lượng tế bào, bám sát hành lang pháp lý sẽ tạo điều kiện cung cấp nguồn tế bào gốc đạt chuẩn, từ đó mang lại kết quả điều trị cao hơn.
NGUỒN THAM KHẢO
- (1): Jian Chen. 2013. “Studies on Culture and Osteogenic Induction of Human Mesenchymal Stem Cells under CO2-Independent Conditions.” PubMed Central. https://pmc.ncbi.nlm.nih.gov/articles/PMC3634141/.
- (2): “Thiết lập quy trình thu nhận tế bào gốc trung mô từ mô mỡ thỏ.” 2021. Y Học TP. Hồ Chí Minh 25 (1 * 2021). https://tapchiyhoctphcm.vn/upload/2021/T25%20S1%202021%20CDHA,%20SHPT%20%28goi%20HDGS%202022%29/163.pdf.
- (3): Christina McKee. 2017. “Advances and challenges in stem cell culture.” ScienceDirect. https://www.sciencedirect.com/science/article/pii/S0927776517304630#abs0010.
- (4): Aleksandra Górska. 2024. “Navigating stem cell culture: insights, techniques, challenges, and prospects.” Frontiers. https://www.frontiersin.org/journals/cell-and-developmental-biology/articles/10.3389/fcell.2024.1435461/full#s5.
HỆ THỐNG Y TẾ CHUYÊN SÂU Y HỌC TÁI TẠO VÀ TRỊ LIỆU TẾ BÀO MESCELLS | MSC
- Hotline: 0866 022 097
- Địa chỉ: TT21, số 204 Nguyễn Tuân, phường Thanh Xuân, Hà Nội, Việt Nam.
- Fanpage: Viện Nghiên Cứu Ứng Dụng Công Nghệ Tế Bào Mescells
Lưu ý: Nội dung bài viết được tổng hợp và tham khảo từ các báo cáo khoa học, tạp chí y khoa uy tín trên thế giới. Tuy nhiên, các thông tin này chỉ mang tính chất tham khảo, không thay thế cho việc chẩn đoán hoặc điều trị y khoa chuyên sâu từ bác sĩ.