Biệt hóa tế bào gốc: Cơ chế và các yếu tố ảnh hưởng đến quá trình biệt hóa
Tế bào gốc có tiềm năng biệt hóa thành nhiều loại tế bào khác nhau và thể hiện khả năng tái tạo nhiều loại mô, cả trong thực nghiệm và lâm sàng. Sự biệt hóa của tế bào gốc có thể được điều chỉnh bởi nhiều tín hiệu khác nhau, bao gồm tín hiệu yếu tố tăng trưởng hòa tan, tín hiệu bám dính tế bào và tín hiệu cơ học. Ở bài viết này, Mescells sẽ trình bày rõ hơn về các loại tế bào gốc và khả năng biệt hóa, cơ chế biệt hóa, các yếu tố ảnh hưởng và ứng dụng của biệt hóa tế bào gốc trong y học.
1. Biệt hóa tế bào gốc là gì?
Sự biệt hóa tế bào gốc là quá trình sinh học mà qua đó các tế bào gốc chưa chuyên hóa có được các chức năng chuyên biệt, biến đổi thành các loại tế bào cụ thể (ví dụ: tế bào thần kinh, cơ hoặc máu). Quá trình này được điều chỉnh bởi các tín hiệu di truyền, hóa học và môi trường, cho phép các tế bào kích hoạt các bộ gen cụ thể đồng thời vô hiệu hóa các bộ gen khác.
Biệt hóa tế bào gốc rất quan trọng cho việc tái tạo mô và được sử dụng trong liệu pháp tế bào gốc để tạo ra các loại tế bào cụ thể. Quá trình này được xem là chìa khóa cho y học tái tạo và nghiên cứu bệnh tật.
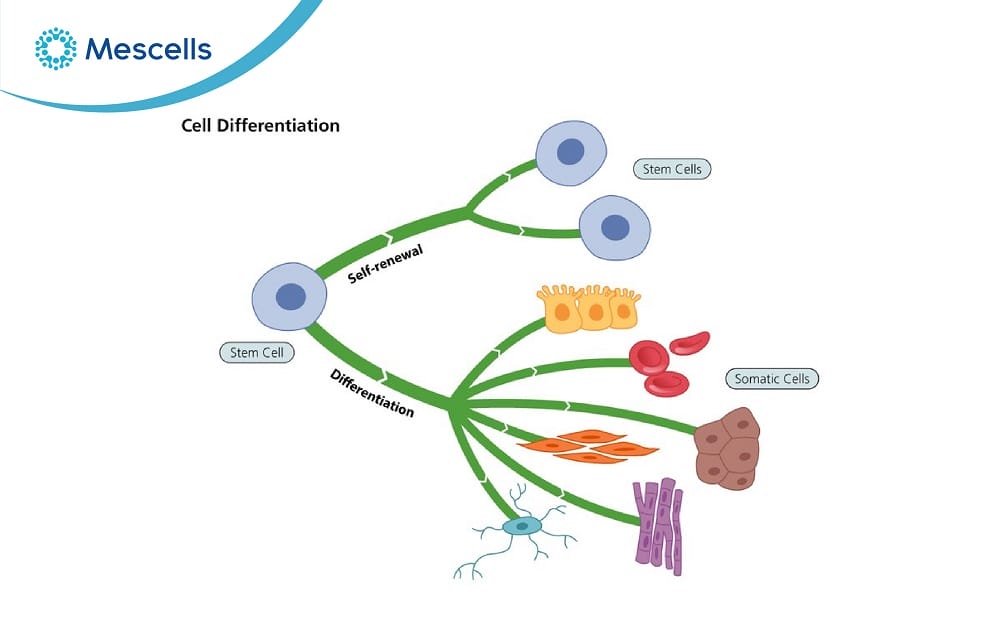
Biệt hóa là một trong hai đặc tính quan trọng của tế bào gốc
2. Các loại tế bào gốc và khả năng biệt hóa
Tế bào gốc có thể được phân loại theo tiềm năng biệt hóa cũng như nguồn gốc của chúng.
Tế bào gốc toàn năng (Totipotent Stem Cells – TSCs): Loại tế bào này có tiềm năng biệt hóa cao nhất thành, có khả năng phát triển thành một cơ thể hoàn chỉnh, bao gồm cả mô phôi và mô ngoài phôi (như nhau thai). Chúng có thể biệt hóa thành tất cả các dòng tế bào cần thiết cho người trưởng thành (1).
Tế bào gốc vạn năng (Pluripotent Stem Cells – PSCs): Chúng có thể biệt hóa thành hầu hết các tế bào của ba lớp mầm (nội bì, trung bì và ngoại bì) nhưng không thể biệt hóa thành các mô ngoài phôi.
- Tế bào gốc phôi (ESC): Được tạo ra từ phôi ở giai đoạn đầu (phôi nang).
- Tế bào gốc đa năng cảm ứng (iPSC): Các tế bào soma trưởng thành được lập trình lại để hoạt động giống như tế bào gốc phôi (ESC).
Tế bào gốc đa năng (Multipotent Stem Cells): Đây là những tế bào chuyên biệt hơn, có khả năng phát triển thành một số loại tế bào nhất định trong một dòng tế bào hoặc mô cụ thể. Chúng có thể biệt hóa thành cả ba lớp mầm.
- Tế bào gốc tạo máu (HSC): Được tìm thấy trong tủy xương, có thể biệt hóa thành nhiều loại tế bào máu khác nhau.
- Tế bào gốc trung mô (MSC): Được lấy từ tủy xương, mô mỡ hoặc dây rốn, có thể phát triển thành tế bào xương, sụn hoặc tế bào mỡ.
- Tế bào gốc thần kinh (NSC): Được tìm thấy trong não, biệt hóa thành tế bào thần kinh, tế bào hình sao và tế bào oligodendroglia.
Tế bào gốc ít tiềm năng (Oligopotent Stem Cells): Chúng chỉ có thể biệt hóa thành một vài loại tế bào, ít hơn so với tế bào đa tiềm năng (multipotent cells).
Tế bào gốc đơn năng (Unipotent Stem Cells): Những tế bào này chỉ có thể biệt hóa thành một loại tế bào duy nhất nhưng vẫn có khả năng tự tái tạo.
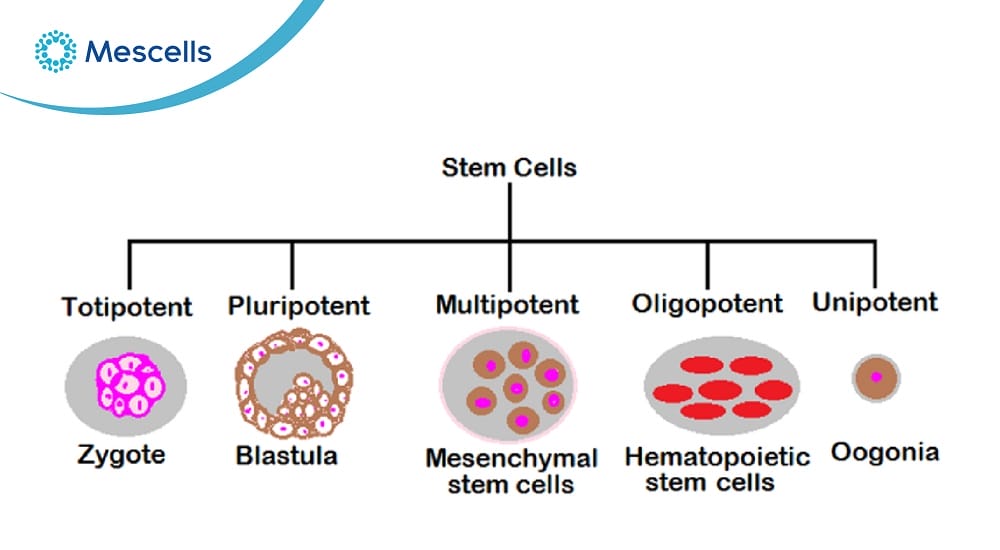
Phân loại tế bào gốc dựa trên tiềm năng biệt hóa
3. Cơ chế biệt hóa tế bào gốc
Bước 1: Nhận tín hiệu
Quá trình biệt hóa bắt đầu khi tế bào gốc nhận các tín hiệu từ môi trường bên ngoài như cytokine và yếu tố tăng trưởng. Những tín hiệu này gắn lên thụ thể trên bề mặt tế bào và kích hoạt các con đường truyền tín hiệu nội bào như Wnt/β-catenin, Notch hoặc MAPK/ERK.
Bước 2: Thay đổi chương trình gen
Sau khi được kích hoạt, các tín hiệu nội bào sẽ đưa các yếu tố phiên mã vào nhân tế bào. Các yếu tố duy trì tính đa năng như Oct4, Sox2, Nanog giảm dần hoạt động, trong khi các yếu tố đặc hiệu cho từng dòng tế bào như MyoD, NeuroD hoặc Nestin được hoạt hóa. Từ đó, tế bào bắt đầu “bật” các gen biệt hóa và “tắt” các gen đa năng.
Bước 3: Điều hòa biểu sinh
Song song với thay đổi gen, tế bào trải qua các biến đổi biểu sinh để duy trì hướng biệt hóa. ADN methylation sẽ “khóa” các gen liên quan đến tính đa năng, trong khi các biến đổi histone giúp “mở” các gen đặc hiệu của tế bào mới. Nhờ vậy, chương trình biệt hóa được duy trì ổn định và lâu dài.
Bước 4: Thay đổi cấu trúc tế bào
Khi quá trình biệt hóa tiếp tục, bộ xương tế bào được tái tổ chức thông qua các con đường như RhoA/ROCK. Điều này làm thay đổi hình dạng và cấu trúc của tế bào. Ví dụ, tế bào thần kinh phát triển các nhánh dài, còn tế bào xương trở nên cứng và giàu chất nền.
Bước 5: Hình thành chức năng chuyên biệt
Ở giai đoạn cuối, tế bào bắt đầu tạo ra các protein đặc hiệu và đảm nhận chức năng riêng. Tế bào thần kinh biểu hiện các protein như neurofilament để dẫn truyền tín hiệu, trong khi tế bào xương tạo collagen và các thành phần khoáng hóa. Lúc này, tế bào gốc đã hoàn tất quá trình biệt hóa thành một tế bào chuyên biệt.
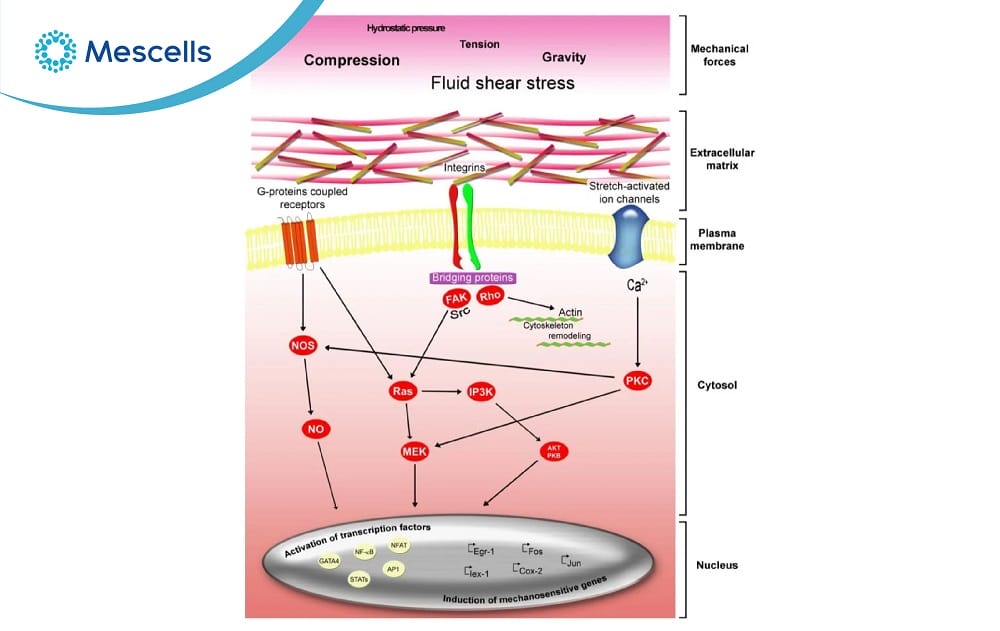
Biệt hóa tế bào gốc bắt đầu khi chúng nhận các tín hiệu từ môi trường bên ngoài như cytokine và yếu tố tăng trưởng
4. Các yếu tố ảnh hưởng đến quá trình biệt hóa
Các phân tử truyền tín hiệu và yếu tố tăng trưởng
Các cytokine và yếu tố tăng trưởng là tín hiệu quan trọng quyết định tế bào gốc sẽ biệt hóa theo hướng nào. Ví dụ, TGF-β1 thúc đẩy hình thành tế bào sụn, BMP-2 và BMP-4 kích thích biệt hóa thành tế bào xương, còn FGF-2 và NGF hỗ trợ phát triển tế bào thần kinh. Trong quá trình này, Runx2 điều khiển biệt hóa xương, còn Sox9 đóng vai trò thiết yếu trong quá trình biệt hóa sụn và được coi là dấu hiệu sớm của sự hình thành tế bào sụn (2).
Tín hiệu cơ học
Độ cứng của bề mặt nuôi cấy có ảnh hưởng lớn đến hướng biệt hóa. Giá thể có độ cứng khoảng 30-40 kPa thường thúc đẩy tế bào gốc phát triển thành tế bào xương, trong khi giá thể mềm khoảng 0,1-1 kPa phù hợp hơn cho biệt hóa thần kinh. Ngoài ra, các lực cơ học như lực kéo hoặc dòng chảy cũng có thể tác động đến quá trình này.
Ma trận ngoại bào (ECM)
Các thành phần của ma trận ngoại bào cung cấp tín hiệu giúp định hướng biệt hóa. Collagen type I thường thúc đẩy hình thành tế bào xương, laminin hỗ trợ biệt hóa thần kinh, còn fibronectin liên quan đến biệt hóa tế bào cơ. Tế bào cảm nhận những tín hiệu này thông qua các protein bám dính trên bề mặt.
Tương tác giữa các tế bào
Các tế bào gốc không hoạt động riêng lẻ mà liên tục trao đổi tín hiệu với nhau. Thông qua con đường Notch-Delta hoặc các phân tử kết dính như cadherin, tế bào này có thể “truyền tín hiệu” cho tế bào khác, từ đó phối hợp và điều chỉnh quá trình biệt hóa.
Điều kiện môi trường nuôi cấy
Nồng độ oxy, độ pH và nguồn dinh dưỡng đều ảnh hưởng đến khả năng biệt hóa. Mức oxy thấp khoảng 2-5% giúp duy trì đặc tính của tế bào gốc tốt hơn. Đồng thời, môi trường nuôi cấy cần được giữ ở pH 7,2-7,4 và cung cấp đầy đủ glucose, axit amin để tế bào phát triển ổn định.
Chu kỳ tế bào
Tế bào gốc có khả năng biệt hóa tốt nhất khi đang ở giai đoạn G1 của chu kỳ tế bào. Đây là thời điểm tế bào “sẵn sàng” tiếp nhận tín hiệu và chuyển sang một loại tế bào chuyên biệt.
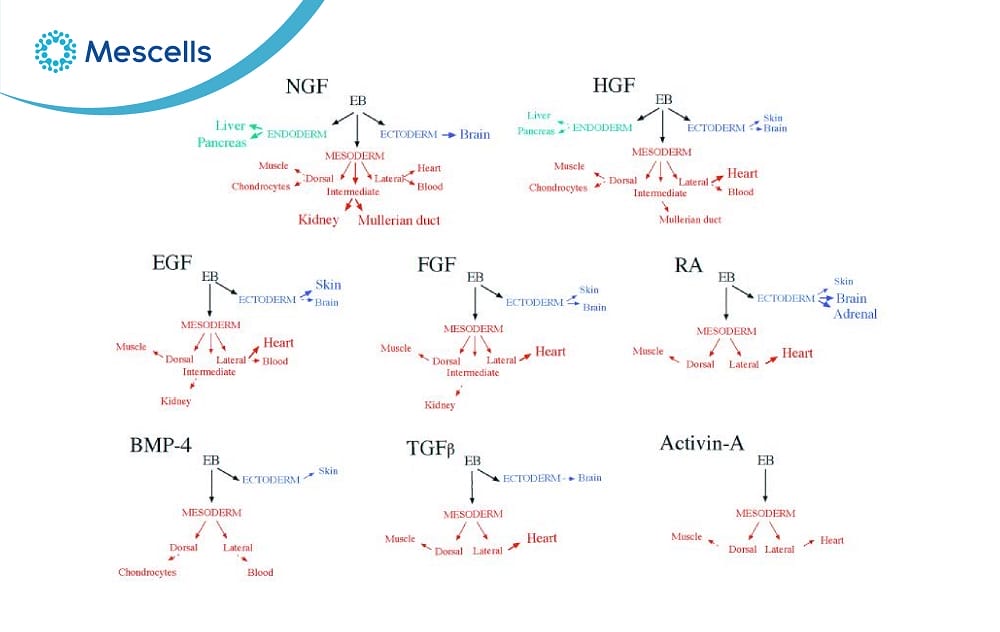
Hình minh họa về tác động của các yếu tố tăng trưởng khác nhau lên quá trình biệt hóa tế bào gốc phôi người trong ống nghiệm
5. Ứng dụng của biệt hóa tế bào gốc trong y học
Trong y học, việc biệt hóa tế bào gốc cho phép tạo ra các tế bào chức năng cụ thể để tái tạo các mô bị tổn thương, mô hình hóa bệnh tật và sàng lọc thuốc mới. Các ứng dụng chính bao gồm:
Tái tạo tế bào tạo máu điều trị các bệnh huyết học
Sử dụng tế bào gốc tạo máu (HSC) từ tủy xương hoặc máu dây rốn để tái tạo toàn bộ hệ thống máu và miễn dịch, đặc biệt là đối với bệnh bạch cầu, u lympho và thiếu máu bất sản.
Y học tái tạo (liệu pháp tế bào)
Tế bào gốc sau khi được biệt hóa có thể dùng để điều trị một số bệnh lý như:
- Rối loạn thần kinh: Phân hóa tế bào gốc thành tế bào thần kinh để điều trị bệnh Parkinson, bệnh Alzheimer và chấn thương tủy sống.
- Tim mạch: Tạo ra các tế bào cơ tim để sửa chữa tổn thương sau suy tim.
- Đái tháo đường: Phát triển các tế bào đảo tụy để sản xuất insulin cho bệnh nhân đái tháo đường type 1.
- Phục hồi hệ cơ xương khớp: Sử dụng tế bào gốc trung mô (MSCs) để biệt hóa thành sụn, xương và mô mỡ nhằm phục hồi các tổn thương và điều trị các bệnh cơ xương khớp.
- Tái tạo võng mạc: Sửa chữa biểu mô sắc tố võng mạc để điều trị thoái hóa điểm vàng do tuổi tác.
Mô hình hóa bệnh tật và phát triển thuốc
- Mô hình hóa bệnh lý: Tạo ra các tế bào gốc vạn năng cảm ứng (iPSC) đặc hiệu cho từng bệnh nhân, được biệt hóa thành các loại tế bào bị ảnh hưởng (ví dụ: tế bào thần kinh trong bệnh Alzheimer) để nghiên cứu cơ chế và sự tiến triển của bệnh.
- Sàng lọc thuốc/Độc tính học: Thử nghiệm các loại thuốc mới trên tế bào gan (hepatocytes) hoặc tế bào cơ tim (cardiomyocytes) của người để đánh giá hiệu quả và độ an toàn, giảm sự phụ thuộc vào mô hình động vật.
Kỹ thuật mô và điều hòa miễn dịch
- In sinh học 3D: Kết hợp các tế bào gốc đã biệt hóa với khung đỡ để tạo ra các cấu trúc mô phức tạp dùng làm cơ quan thay thế trong cấy ghép nội tạng.
- Chăm sóc vết thương mạn tính: Sử dụng tế bào gốc trung mô (MSCs) để thúc đẩy tái tạo mô đối với các vết loét bàn chân do đái tháo đường và bỏng.
- Điều hòa miễn dịch: Sử dụng tế bào gốc trung mô (MSCs) để điều trị các bệnh tự miễn và giảm bệnh ghép chống chủ (GVHD).
Thẩm mỹ và làm lành vết thương
Ứng dụng tế bào gốc mô mỡ hoặc tủy xương để tái tạo da, điều trị sẹo…
Nhờ khả năng biệt hóa, tế bào gốc được ứng dụng đa dạng trong y học
Biệt hóa tế bào gốc là một quá trình phức tạp với nhiều cơ chế và bị chi phối bởi nhiều yếu tố. Các yếu tố này có thể thay đổi tùy thuộc vào loại tế bào gốc và môi trường tế bào cụ thể. Nhiều nghiên cứu về đặc tính biệt hóa của tế bào gốc vẫn đang được tiến hành liên tục và không ngừng cải tiến nhằm mở rộng phạm vi ứng dụng của tế bào gốc trong các lĩnh vực y học khác nhau.
Hiểu biết về quá trình biệt hóa giúp các nhà khoa học, sinh học có thêm một góc nhìn mới về sinh lý học tế bào gốc, cung cấp thêm nền tảng cho các ứng dụng như y học tái tạo và liệu pháp tế bào, hứa hẹn nhiều phương pháp điều trị hiệu quả hơn trong tương lai.
NGUỒN THAM KHẢO
- (1): Poliwoda, Salomon. 2022. “Stem cells: a comprehensive review of origins and emerging clinical roles in medical practice.” PMC. https://pmc.ncbi.nlm.nih.gov/articles/PMC9404248/.
- (2): Yi Peng. 2003. “Factors affecting osteogenesis and chondrogenic differentiation of mesenchymal stem cells in osteoarthritis.” PMC. https://pmc.ncbi.nlm.nih.gov/articles/PMC10324504/#sec2.
HỆ THỐNG Y TẾ CHUYÊN SÂU Y HỌC TÁI TẠO VÀ TRỊ LIỆU TẾ BÀO MESCELLS | MSC
- Hotline: 0866 022 097
- Địa chỉ: TT21, số 204 Nguyễn Tuân, phường Thanh Xuân, Hà Nội, Việt Nam.
- Fanpage: Viện Nghiên Cứu Ứng Dụng Công Nghệ Tế Bào Mescells
Lưu ý: Nội dung bài viết được tổng hợp và tham khảo từ các báo cáo khoa học, tạp chí y khoa uy tín trên thế giới. Tuy nhiên, các thông tin này chỉ mang tính chất tham khảo, không thay thế cho việc chẩn đoán hoặc điều trị y khoa chuyên sâu từ bác sĩ.